ТЕМА 1. ПОЧАТКОВІ ХІМІЧНІ ПОНЯТТЯ
Урок 19. Узагальнення і систематизація знань
Цілі: узагальнити набуті знання, вміти використовувати їх під час виконання завдань різного типу.
Обладнання: періодична таблиця хімічних елементів.
Тип уроку: узагальнююче повторення.
Форми роботи: хімічна розминка, самостійна робота, робота в групах, прес-конференція.
ХІД УРОКУ
I. Організація класу
II. Оголошення теми й мети уроку
III. Актуалізація опорних знань
Учні одразу сідають групами. На дошці записані прості завдання,
1. Де у формулі K2Cr2O7 індекси? Що вони означають?
2. Як називається й що означає цифра перед формулою вуглекислого газу?
5CO2
3. Запишіть формулу речовини, що складається з двох атомів Натрію, одного атома Сульфуру й чотирьох атомів Оксигену.
4. Відносні атомні маси Кальцію, Карбону й Оксигену відповідно дорівнюють 40, 12 і 16. Яка відносна молекулярна маса речовини CaCO3?
IV. Самостійна робота на картках
1. Доберіть коефіцієнти в рівняннях.
І варіант

ІІ варіант

ІІІ



IV варіант
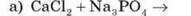


2. Закінчіть хімічні рівняння. Допишіть, де треба, формули й доберіть коефіцієнти.
І варіант

ІІ варіант

III варіант

IV варіант

V. Робота в групах
Завдання групам
1. Обчисліть масові частки Сульфуру в речовинах, формули яких FeS і SO2. В якій формулі масова частка Сульфуру менша?
2. Випишіть окремо фізичні й хімічні явища:
А) замерзання води;
Б) іржавіння заліза;
В) танення сніжинок;
Г) пожовтіння листя;
Д) скисання молока;
Е) загнивання м’яса;
Ж) кування заліза.
3. Яка ознака хімічної реакції взаємодії соди з оцтом? Які ще ознаки хімічних реакцій ви знаєте?
4. Яка маса води розклалась, якщо в результаті реакції утворилося 64 г кисню і 8 г водню?
5. Доберіть коефіцієнти:

6. Закінчіть рівняння реакцій:

VI. Підбиття підсумків уроку
Прес-конференція (обговорення виконаних завдань)
Два останні завдання доцільно виконати на дошці й таким чином перевірити їх правильність і обговорити помилки. Інші завдання можна перевірити усно, пояснюючи їх виконання.
VII. Домашнє завдання
Підготуватися до тематичного оцінювання.
