ЛАБОРАТОРНИЙ ДОСЛІД № 4
Виготовлення водних розчинів із заданими масовими частками розчинених речовин.
Обладнання: терези, мірний циліндр, скляна паличка, хімічна склянка.
Реактиви: будь-яка наявна в кабінеті хімії розчинна сіль.
Правила безпеки. При проведенні дослідів:
– використовуйте невеликі кількості реактивів;
– остерігайтеся потрапляння реактивів на одяг, шкіру, в очі.
1. Виготовити розчин солі масою 50 г з масовою часткою розчиненої речовини 10%.
Дано:
Маса розчину m = 50 г
Масова частка ω = 10
Mрозчиненої речовини = ?
Mрозчинника = ?
Розв’язання:
Визначимо масу розчиненої речовини:
Mрозчиненої речовини = ω • mрозчину = 0,1 • 50 г = 5 г
Визначимо масу розчинника:
Mрозчинника = 50 г – 5 г = 45 г
Відповідь: mрозчиненої речовини = 5 г; mрозчинника = 45 г.
На ліву шальку терезів поставте хімічну склянку і зважте її. На другу шальку додайте важки так, щоб їхня маса дорівнювала сумарній масі хімічної склянки і солі, необхідної для приготування розчину. У хімічну склянку поміщайте невеликими порціями сіль, доки маси обох шальок терезів не врівноважаться.
У мірний циліндр
4. Вилийте відміряний об’єм води в хімічну склянку до відваженої солі і ретельно перемішайте суміш скляною паличкою до повного розчинення речовини.
Висновки
1. Виготовлення розчинів потребує проведення математичних розрахунків.
2. Для виготовлення розчину порції твердих речовини зважують на терезах.
3. Для відмірювання порції розчинника використовують мірний посуд.
4. Під час виготовлення розчину ретельно перемішують його компоненти.
Контрольні запитання
№ 1. Для вираження складу розчинів часто використовують масову частку розчиненої речовини, що дорівнює відношенню маси розчиненої речовини до маси розчину.
№ 2. Масова частка речовини в розчині показує, яка частина маси розчину припадає на розчинену речовину. Масову частку розчиненої речовини обчислюють за формулою:
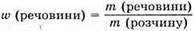
№ 3. Масову частку виражають у частках від одиниці (безрозмірна величина) або у відсотках. Для отримання числа у відсотках необхідно значення масової частки помножити на 100%.
Завдання для засвоєння матеріалу
№ 1.
А) не зміниться, тому що в закритій посудині вода не випаровувається;
Б) зміниться, тому що у відкритій посудині вода випаровувається, зміниться маса розчину.
№ 2.
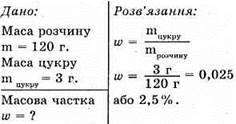
Відповідь: масова частка ω = 0,025 або 2,5%.
№ 3.

Відповідь: mсолі = 7,5 г.
№ 4.

Відповідь: масова частка ω = 0,1 або 10%.
№ 5.

Відповідь: масова частка ω = 0,06%.
№ 6.
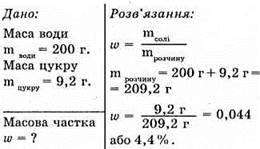
Відповідь: масова частка ω = 4,4%.
№ 7.

Відповідь: mсолі = 12,5 г.
№ 8.

Відповідь: mцукру = 15 г, mводи = 485 г.
№ 9.

Відповідь: mсолі = 90 г, mводи = 9910 г.
ДОМАШНІЙ ЕКСПЕРИМЕНТ
Виготовлення водного розчину кухонної солі
Речовини та обладнання: терези, аркуш паперу, мірна посудина, 2 хімічні стакани на 250 мл, мірна ложечка для набирання сипучих речовин, скляна паличка, цукор, дистильована вода.
Розрахунки
Завдання 1. Виготовити водний розчин кухонної солі з масовою часткою розчиненої речовини 8 %, взявши для цього воду об’ємом 1,5 л.
Дано:
Об’єм розчину V = 1,5 л.
Густина ρ = 1 г/мл.
Масова частка ω = 8 % = 0,08.
Mрозчиненої речовини = ?
Mрозчинника = ?
Розв’язання:
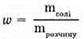
Визначимо масу розчину:
Mрозчину = 1500 мл • 1 г/мл = 1500 г
Визначимо масу розчиненої речовини:
Mрозчин. речов. = ω • mрозчину = 0,08 • 1500 г = 120 г
Визначимо масу розчинника:
Mрозчинника = 1500 г – 120 г = 1380 г
Відповідь: mрозчиненої речовини = 120 г; mрозчинника = 1380 г.
Так як 1 столова ложка містить 30 г кухонної солі, а чайна ложка – 10 г, відмірюємо 120 г кухонної солі (4 столових ложки або 12 чайних ложок).
Висновки
1. Виготовлення розчинів потребує проведення математичних розрахунків.
2. Для виготовлення розчину порції твердих речовини зважують на терезах.
3. Для відмірювання порції розчинника використовують мірний посуд.
4. Під час виготовлення розчину ретельно перемішують його компоненти.
