ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання
РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ
4. Хімічна реакція
4.9. Оборотність хімічних реакцій
За цією ознакою розрізняють:
– реакції, які за однакових умов відбуваються у двох протилежних напрямках, називають оборотними. Наприклад, реакція синтезу сульфур(VI) оксиду (знак  вказує саме на оборотність реакції):
вказує саме на оборотність реакції):

– необоротними називають реакції, які відбуваються тільки в одному напрямку та завершуються повним
Більшість хімічних реакцій є оборотними (принципово всі реакції є оборотними; необоротними їх умовно називають тоді, коли для здійснення зворотної реакції потрібно створити екстремальні умови).
4. 9.1. Хімічна рівновага
Під час проходження оборотних реакцій можна виділити кілька етапів:

1. На початку проходження прямої реакції швидкість прямої реакції є максимальною й описується таким кінетичним рівнянням:
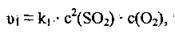
Де V1 – це швидкість прямої реакції,
K1 – константа швидкості прямої
C2(SO2) – концентрація сульфур(ІV) оксиду в степені, що дорівнює стехіометричному коефіцієнту,
С(O2) – концентрація кисню.
Швидкість зворотної реакції V2 у початковий момент реакції описують кінетичним рівнянням:
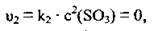
Тому що сульфур(VІ) оксиду в початковій суміші немає.
2. У міру проходження реакції поступово швидкість прямої реакції зменшується, тому що SO2 і O2 взаємодіють і їхні концентрації знижуються. При цьому швидкість зворотної реакції поступово збільшується, тому що збільшується концентрація сульфур(VI) оксиду – SO3.
3. Урешті наступає такий момент, коли швидкості прямої і зворотної реакцій стануть однаковими.
Такий стан системи називають хімічною рівновагою. Отже, стан реакційної системи, при якому швидкість прямої реакції дорівнює швидкості зворотної реакції, – це хімічна рівновага.
Описані етапи оборотної реакції можна показати і графічно:

Рис. Зміна швидкості прямої (v1) і зворотної (v2) реакції системи з часом (τ)
Хімічна рівновага є динамічною (рухомою). У стані хімічної рівноваги продовжують відбуватись обидві реакції – і пряма, і зворотна. Оскільки швидкості цих реакцій рівні, концентрації всіх речовин у реакційній системі не змінюються. Такі концентрації речовин називають рівноважними.
У стані хімічної рівноваги за, одиницю часу утворюється така ж кількість молекул SO3, яка й перетворюється назад на SO2 і O2.
Стан рівноваги оборотного процесу характеризується константою рівноваги. Для оборотної реакції, записаної в загальному вигляді
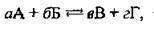
Де А, Б, В, Г – речовини,
А, б, в, г – стехіометричні коефіцієнти, запишемо кінетичні рівняння для швидкості прямої (v1) і для зворотної (v2) реакцій у момент хімічної рівноваги:

Де, , , – рівноважні концентрації речовин А, Б, В, Г,
А, б, в, г – стехіометричні коефіцієнти,
K1 і k2 – константи швидкостей прямої та зворотної реакцій.
Оскільки за умов рівноваги v1 = v2, то

Оскільки k1 і k2 є константами, то і  – величина стала. Її назвали константою рівноваги.
– величина стала. Її назвали константою рівноваги.
Константа рівноваги К – це відношення швидкостей зворотної та прямої реакцій.
За її значенням можна встановити відносний вихід продуктів реакції: що більше значення константи рівноваги, то повніше вихідні речовини перетворюються в продукти реакції, а тому вихід продуктів більший. Якщо ж значення константи рівноваги мале, то вихід продуктів реакції малий.
Якщо умови, за яких наступила рівновага, не змінювати, то рівновага може існувати як завгодно довго. Стан хімічної рівноваги залежить від трьох величин:
– концентрації речовин, що є в системі;
– температури;
– тиску, якщо в реакції беруть участь гази.
Якщо ж замінюється хоча б одна з цих величин, хімічна рівновага (яка є рухомою) зміщується. Змінюються й концентрації всіх речовин, які беруть участь у реакції; змінюються до встановлення нової хімічної рівноваги.
Процес зміни концентрацій унаслідок порушення рівноваги називають зміщенням рівноваги. Якщо ж при цьому збільшується концентрація речовин у правій частині рівняння, то кажуть, що рівновага зміщується праворуч. І навпаки, якщо збільшується концентрація речовин у лівій частині рівняння, кажуть, що, рівновага зміщується ліворуч.
Зміщення хімічної рівноваги, тобто перехід від одного рівноважного стану до іншого, що відповідає зміненим умовам, підкоряється правилу, яке називають принципом Лe Шательє (1884)2: якщо змінити одну з умов, за яких система перебуває в рівновазі – температуру, тиск чи концентрацію речовин, – то рівновага зміщується в напрямку тієї реакції, яка протидіє цій зміні.
Вплив зміни температури
Розгляньмо оборотну реакцію синтезу аміаку:

Пряма реакція (синтез аміаку) є екзотермічною реакцією, а зворотна (розклад аміаку) відповідно ендотермічною. Підвищення температури зміщує рівновагу в бік проходження ендотермічної реакції, а зниження температури – в бік екзотермічного процесу. Отже, для цієї реакції з метою зміщення рівноваги праворуч температуру потрібно знижувати.
Вплив тиску
При підвищенні тиску збільшується кількість молекул в одиниці об’єму газової суміші. Та з реакцій (пряма чи зворотна), яка відбувається за участі більшої кількості молекул газоподібних речовин, протікає швидше. Відбувається зміна швидкостей реакцій, і, нарешті, знову наступає хімічна рівновага.
Зауважимо, що реакція, яка відбувається зі збільшенням кількості молекул газів, приводить до підвищення тиску в системі, а реакція, що відбувається зі зменшенням кількості молекул газів, – до зниження тиску.
Отже, при підвищенні тиску рівновага зміщується в бік зменшення кількості молекул газоподібних речовин, тобто в бік зниження тиску. А при зниженні тиску рівновага зміщується в бік зростання кількості молекул газоподібних речовин, тобто в бік підвищення тиску.
У наведеному вище прикладі синтезу аміаку:

(у лівій частині маємо чотири об’єми газу, а в правій – два) підвищення тиску приведе до зміщення рівноваги праворуч. Якщо ж під час реакції загальна кількість молекул (а отже, й об’єм) газоподібних речовин не змінюється, стан рівноваги від зміни тиску не залежить.
Вплив концентрації
Якщо в рівноважну систему вводиться будь-яка речовина, що бере участь у реакції (концентрація збільшується), то рівновага зміщується в бік тієї реакції, під час проходження якої дана речовина витрачається. Якщо ж з рівноважної системи виводиться речовина, то рівновага зміщується в бік тієї реакції, при перебігу якої дана речовина утворюється. Так, наприклад, для реакції

З метою зміщення рівноваги праворуч (у бік прямої реакції) необхідно в рівноважну суміш вводити SО2 і О2, тобто збільшувати їхні концентрації і виводити з рівноважної суміші, зменшувати концентрацію SО3.
Приклад. Поміркуйте, в який бік зміститься рівновага реакції

Якщо: а) збільшити температуру;
Б) зменшити концентрацію вуглекислого газу СО2;
В) збільшити тиск у системі.
Відповідь: а) пряма реакція є екзотермічною, а зворотна – ендотермічною. Підвищення температури зміщує рівновагу в бік ендотермічної реакції, тобто ліворуч; б) зменшення концентрації вуглекислого газу приведе до зміщення рівноваги в бік реакції його утворення, тобто праворуч; в) рівняння реакції показує, що один об’єм СО реагує з одним об’ємом водяної пари (разом два об’єми), утворюючи 1 об’єм СО2 і 1 об’єм Н2 (також два об’єми). Отже, кількість молекул газоподібних речовин у системі не змінюється і підвищення чи зниження тиску не приведе до зміщення рівноваги.
_________________________________________________________
1 Константа швидкості реакції (питома швидкість реакції) – коефіцієнт пропорційності в хімічному рівнянні. Фізичний зміст константи швидкості реакції k випливає з рівняння закону діючих мас; k чисельно дорівнює швидкості реакції, коли концентрації кожної з речовин, що реагують, є постійними і становлять 1 моль/л. Отже, k не залежить від концентрації, а лише від природи реагентів.
2 Французький фізико-хімік Анрі Лe Шательє (1850-1936) сформулював цей термодинамічний принцип, а дещо пізніше німецький фізик Карл Браун (1850-1918) його узагальнив.
