І СЕМЕСТР
Тема 2. ВУГЛЕВОДНІ
Урок 10
Тема уроку. Поняття про циклоалкани (циклопарафіни)
Цілі уроку: розширити знання учнів про вуглеводні на прикладі будови та властивостей циклоалканів; розвивати вміння складати структурні формули органічних сполук, їхні назви за систематичною номенклатурою на прикладі ізомерів циклоалканів; ознайомити з явищем міжкласової ізомерії на прикладі циклоалканів; формувати знання учнів про хімічні властивості циклоалканів як насичених вуглеводнів, головні способи одержання циклоалканів,
Тип уроку: комбінований урок засвоєння знань, умінь і навичок і творчого застосування їх на практиці.
Форми роботи: розповідь учителя, евристична бесіда, демонстраційний експеримент.
Обладнання: моделі циклопентану й циклогексану.
ХІД УРОКУ
I. Організація класу
II. Актуалізація опорних знань.
Мотивація навчальної діяльності
1. Двоє учнів біля дошки виконують схеми перетворень:
А) етан 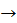 брометан
брометан 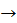 бутан
бутан 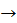 ізобутан
ізобутан 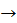 карбон(IV) оксид;
карбон(IV) оксид;
Б) C3H8 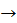
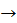 C6H14
C6H14 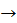 C6H12
C6H12 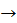 CO2
CO22. Обчисліть кількість теплоти, що виділиться внаслідок спалювання 1 м3 суміші метану, етану і пропану складу 65, 25 і 10 % відповідно (об’єми приведено до н. у.).
3. Зобразіть формулу вуглеводню складу C5H10, якщо відомо, що в молекулі всі зв’язки між атомами Карбону – одинарні.
III. Вивчення нового матеріалу
1. Циклоалкани (циклопарафіни)
Розповідь учителя
На відміну від насичених вуглеводнів, що характеризуються наявністю відкритих карбонових ланцюгів, існують вуглеводні із замкнутими ланцюгами (циклами). За своїми властивостями вони нагадують звичайні насичені вуглеводні алкани (парафіни), звідси й походить їхня назва – циклоалкани (циклопарафіни). Загальна формула гомологічного ряду циклоалканів – CnH2n, тобто циклоалкани ізомерні етиленовим вуглеводням. Представниками цього ряду сполук є циклопропан, циклобутан, циклопентан, циклогексан.

Дуже часто в органічній хімії структурні формули перелічених циклоалканів зображують без символів C і H простими геометричними фігурами: 
2. Ізомерія
Для циклопарафінів, починаючи із C4H8, характерними є деякі види структурної ізомерії, пов’язані:
А) з числом атомів Карбону в кільці, наприклад:  (етилциклопропан),
(етилциклопропан),  (метилциклобутан);
(метилциклобутан);
Б) з числом атомів Карбону в замісниках:  (1-метил-2-пропілциклопентан),
(1-метил-2-пропілциклопентан),  (1,2-діетилциклопентан);
(1,2-діетилциклопентан);
В) з положенням замісника в кільці:  (1,1-диметилциклогексан),
(1,1-диметилциклогексан),  (1,2-диметилциклогексан).
(1,2-диметилциклогексан).
Для циклоалканів характерною є також міжкласова ізомерія з алкенами.
Завдання 1. Складіть і назвіть ізомери циклоалкану складу C6H12.
За наявності двох замісників у кільці біля різних атомів Карбону можлива геометрична цис-транс-ізомерія, починаючи із C5H10, і оптична ізомерія. Оптична ізомерія виявляється в тому випадку, якщо молекула не має площини симетрії. (Демонструємо відео-фрагмент або схему утворення цис-транс-ізомерії в циклічних сполуках.)
Для циклогексану, як правильного шестикутника, між’ядерні кути становлять 120°. Якби молекула циклогексану мала плоску будову, то відхилення від нормального валентного кута атома Карбону становило б: 109,5°-120° = 10,5°.
Циклогексан і більші цикли мають неплоску будову. У розглянутій молекулі циклогексану зберігаються звичайні валентні кути за умови його існування у двох конформаціях – “крісла” і “ванни”. Конформація “крісла” менш напружена, тому циклогексан існує переважно у вигляді конформерів I і III, причому цикл зазнає безперервної інверсії (від лат. inversio – “перекидання”, “перестановка”) з проміжним утворенням конформера II:

3. Способи одержання циклоалканів
1) Одним з найчастіше застосовуваних способів одержання циклоалканів є циклізація дигалогенопохідних вуглеводнів: а) у результаті дії цинку в етиловому спирті на відповідне дигалогенопохідне ланцюг атомів Карбону замикається, приводячи до утворення циклоалкану (Г. Густавсон):

Б) унаслідок дії амальгами літію на 1,4-дибромбутан утворюється циклобутан:

2) Гідрогенізація ароматичних сполук:

Завдання 2. Одержіть циклопентан з 1,5-дихлорпентану.
4. Фізичні властивості циклоалканів
Циклоалкани мають більш високі температури плавлення і кипіння й більшу густину, ніж відповідні алкани. За однакового складу температура кипіння циклопарафіну тим вища, чим більший розмір циклу. Циклоалкани у воді практично не розчиняються, однак розчиняються в органічних розчинниках.
Завдання 3. Порівняйте фізичні властивості деяких циклоалканів, наведених у таблиці.
Фізичні властивості деяких циклоалканів
Сполука | T°пл, °С | T°кип, °С | D420 |
Циклопропан | -126,9 | -33 | 0,6881 |
Метилциклопропан | -177,2 | 0,7 | 0,69122 |
Циклобутан | -80 | 13 | 0,7038 |
Метилциклобутан | -149,3 | 36,8 | 0,6931 |
Циклопентан | -94,4 | 49,3 | 0,7460 |
Метилциклопентан | -142,2 | 71,9 | 0,7488 |
Циклогексан | 6,5 | 80,7 | 0,7781 |
1За температури кипіння. 2За температури -20,0 °С |
5. Хімічні властивості
Хімічні властивості циклопарафінів залежать від числа атомів Карбону, що становлять цикл. Нижчі циклоалкани (циклопропан і циклобутан) поводяться як ненасичені вуглеводні, вони здатні вступати в реакції приєднання. Циклоалкани з більшою кількістю атомів Карбону в циклі поводяться як алкани, для них характерними є реакції заміщення.
¦ Як ви вважаєте, чому?
1) Гідрування
У процесі каталітичного гідрування три-, чотири – та п’ятичленні цикли розриваються з утворенням алканів:

Як бачимо, п’ятичленний цикл розривається лише за високих температур.
2) Галогенування
Тричленний цикл під час галогенування розривається, приєднуючи атоми галогену:

Циклопарафіни з п’яти – й шестичленними циклами в процесі галогенування вступають у звичайні для парафінів реакції заміщення:

3) Гідрогалогенування
Циклопропан та його гомологи взаємодіють з галогеноводнями з розривом циклу:

Реакція здійснюється відповідно до правила Марковнікова (решта циклопарафінів з галогеноводнями не реагує).
4) Дегідрування
Сполуки з шестичленними циклами в разі нагрівання з каталізаторами дегідруються з утворенням ароматичних вуглеводнів:

5) Окиснення
Незважаючи на стійкість циклопарафінів до окисників за звичайних умов, у разі нагрівання сильні окисники перетворюють їх на двоосновні карбонові кислоти з тим же числом атомів Карбону.

IV. Підбиття підсумків уроку
1. Застосування циклоалканів
Найбільше практичне значення мають циклогексан та етилциклогексан. Циклогексан використовується для одержання циклогексанолу, циклогексанону, адипінової кислоти, капролактаму, а також як розчинник. Циклопропан застосовується в медичній практиці як інгаляційний анестезуючий засіб.
2. Розв’язання задач
1) Обчисліть об’єм хлору, необхідний для хлорування 5 л циклопропану (н. у.), якщо втрати в синтезі становлять 8 %.
2) Обчисліть масу пентану, що утвориться в результаті гідрування циклопентану масою 140 г.
V. Домашнє завдання
Опрацювати матеріал параграфа, відповісти на запитання до нього, виконати вправи.
