ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ
Частина III. ОРГАНІЧНА ХІМІЯ
Розділ 17. КИСНЕВМІСНІ ОРГАНІЧНІ СПОЛУКИ
§ 17.4. Феноли
Феноли – це органічні сполуки, у молекулах яких гідроксильні групи зв’язані з бензольним ядром.
Вони є похідними ароматичних вуглеводнів. Наприклад:
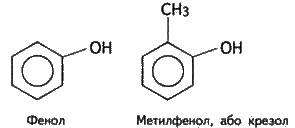
Феноли з однією гідроксильною групою називаються одноатомними, з двома – двохатомними, з трьома – трьохатомними. При побудові номенклатури фенолів прийнято позначати атоми вуглецю у бензольному

Найпростіший фенол С6Н5ОН називається фенолом, або карболовою кислотою. Фенол – безбарвна кристалічна речовина з різким характерним запахом. Під час зберігання він поступово окиснюється киснем повітря і набуває рожевого за барвлення. Фенол плавиться при 42,3 °С, кипить при 182 °С; частково розчиняється у воді (6 г у 100 г води); має сильні антисептичні властивості, тобто здатний вбивати багато мікроорганізмів, дуже отруйний. При потраплянні на шкіру обпікає її, утворюючи пухирі
За хімічними властивостями феноли відрізняються від спиртів. Ця відмінність спричинена взаємним впливом у молекулі фенолу гідроксильної групи і бензольного радикала, який називається фенілом (С6Н5-). Суть цього впливу зводиться до того, що п-електрони бензольного ядра частково залучають до своєї сфери неподілені електронні пари атома кисню гідроксильної групи, внаслідок чого зменшується електронна густина біля атома кисню. Це, у свою чергу, викликає додаткове зміщення електронної густини зв’язку О-Н від водню до кисню, водень набуває кислотних властивостей, стає рухливим і реакційноздатним.
Отже, під впливом фенілу зв’язок атома водню з киснем у гідроксильній групі слабшає, що призводить до часткового відщеплення іонів водню. Фенол виявляє властивості слабкої кислоти (слабшої за вугільну). Тому він легко взаємодіє не лише з металічними натрієм і калієм, а й із їдкими лугами1 , утворюючи феноляти, стійкі у водних розчинах:
2С6Н5OН + 2Na -> 2C6H5ONa + Н2;
С6Н5ОН + NaOH -> C6H5ONa + Н2О.
Оскільки кислотні властивості фенолу виражені дуже слабко, то феноляти (солі фенолу) легко розкладаються мінеральними кислотами, в тому числі й вугільною:
C6H5ONa + СО2 + Н2О -> С6Н5ОН + NaHCO3.
Вплив атомів у молекулах взаємний. Гідроксильна група, в свою чергу, впливає на бензольне ядро, внаслідок чого водневі атоми бензолу стають більш рухливими і легко заміщуються іншими атомами або радикалами. Так, наприклад, фенол без нагрівання і без каталізаторів енергійно взаємодіє з бромом і нітратною кислотою, утворюючи відразу три – заміщені похідні (в положеннях 2, 4 і 6):

Бензол же з бромом та нітратною кислотою взаємодіє лише при нагріванні і наявності каталізаторів.
Під впливом гідроксильної групи полегшується взаємодія фенолу з формальдегідом (див. § 17.8).
У великих кількостях фенол добувають двома способами: з кам’яновугільної смоли, що утворюється під час сухої перегонки вугілля, та – основну масу – синтетично з бензолу і пропілену (“кумольний” спосіб).
Спочатку з бензолу і пропілену добувають ізопропілбензол (кумол):

Кумол – безбарвна рідина, легша за воду, т. кип. 152 °С. Потім кумол піддають рідкофазному каталітичному окисненню киснем повітря:

Сполука, що утворюється (гідропероксид кумолу), під впливом сірчаної кислоти розщеплюється на фенол і ацетон:

Отже, з бензолу і пропілену добувають два цінних продукти – фенол і ацетон. Цей метод розробив російський хімік П. Г. Сергєєв. Кумол є також вихідною речовиною для добування а-метилстиролу, який використовують для виробництва каучуків.
Фенол – сильний антисептик, застосовується як дезінфікуюча речовина. Особливо багато його витрачають для виробництва пластмас – фенопластів. Фенол застосовується для виробництва лікарських речовин, фотографічних проявників і фарб.
1За тих самих умов одноатомні насичені спирти практично не взаємодіють з лугами – рівновага зміщена в бік вихідних речовин (§ 17.1).
